سم بكتيري يحرر الجينات كأول محرر جينات ميتوكوندري
للأسلحة البكتيرية استخدام غير متوقع
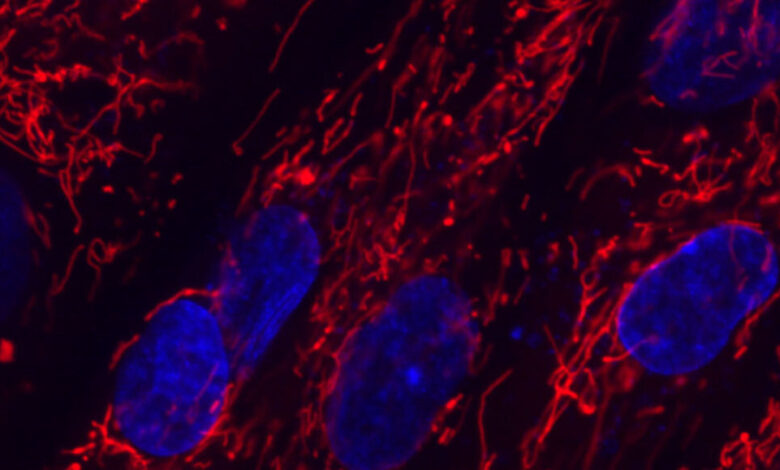
سم بكتيري يحرر الجينات، أعيد تصميم بروتين تفرزه البكتيريا لقتل الميكروبات الأخرى لتعديل الحمض النووي الذي يتعذر الوصول إليه من قبل محرري الجينات الآخرين، حسبما أفاد علماء في دورية Nature. هذا التقدم يمهد الطريق لإصلاح الطفرات في الميتوكوندريا. هذه العضيات المنتجة للطاقة موروثة من الأم ولها حمضها النووي الخاص بها، والتي تختلف عن المعلومات الجينية – من كلا الوالدين – المخزنة في نواة الخلية.
يقول فامسي موثا، الباحث في معهد هوارد هيوز الطبي في مستشفى ماساتشوستس العام في بوسطن ومعهد برود التابع لمعهد ماساتشوستس للتكنولوجيا وجامعة هارفارد: “لقد كنت عالم أحياء ميتوكوندريا لمدة 25 عامًا، وأرى أن هذا تقدم مهم للغاية في هذا المجال” .
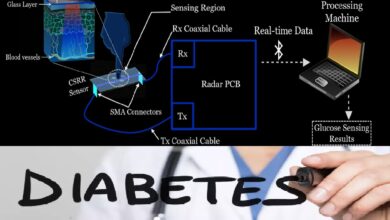
تسبب الطفرات في الحمض النووي للميتوكوندريا أكثر من 150 متلازمة مميزة وتؤثر على 1000 إلى 4000 طفل يولدون في الولايات المتحدة كل عام. لا توجد علاجات لهذه الأمراض حتى يومنا هذا. والطريقة الوحيدة حاليًا لمنع الطفل من وراثة الميتوكوندريا المختلة وظيفيًا هي طريقة “الطفل المكون من ثلاثة أباء” . تتطلب تقنية الإخصاب في المختبر ميتوكوندريا من بويضة متبرعة، بالإضافة إلى معلومات وراثية من الأم و الأب. التقنية لحالية تواجه صعوبات أخلاقية و اعتراضاً من جهات كثيرة.
التقنية المتاحة حالياً
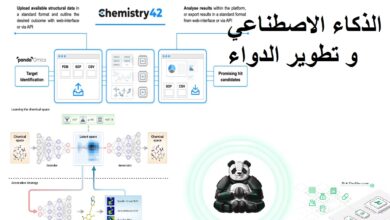
تحرير الجينات هو نهج لتطوير علاجات للأمراض الوراثية ،وهي تقنية تقوم بإجراء تغييرات مباشرة على الحمض النووي. ربما يكون أشهر محرر الجينات ، CRISPR / Cas9 هو مقص جزيئي يقطع الحمض النووي. كما استخدم الباحثون سابقًا أيضًا جزيئات تسمى TALENs لتقطيع الحمض النووي للميتوكوندريا. كانت التجارب في الفئران بهدف القضاء على العضيات المعيبة. تعمل تقنية أحدث، تسمى محررات القاعدة، على تثبيت البروتينات التي يمكنها تغيير قواعد الحمض النووي. تحول تلك القواعد ممثلة بالأحرف A و C و G و T – إلى نسخة معدلة من البروتين المرتبط بـ CRISPR Cas9 (SN:. هؤلاء المحررين يحولون قاعدة DNA إلى أخرى كيميائيًا، ويصلحون بشكل أساسي الأخطاء المطبعية التي يمكن أن تؤدي إلى المرض. ومع ذلك، فإن هذه التقنية تعمل فقط على الحمض النووي في النوى، وليس الميتوكوندريا.
الاكتشاف، صدفة بعد أشهر
ثبت أن السم الذي تفرزه البكتيريا Burkholderia cenocepacia بشكل غير متوقع هو الحل المطلوب لإنشاء محرر قاعدة صديق للميتوكوندريا. استنتج ماركوس دي مورايس، عالم الأحياء الدقيقة بجامعة واشنطن، أن السم يقتل البكتيريا عن طريق التسبب في حدوث طفرات في الحمض النووي. لكن لأشهر، لم يستطع حل الكيفية التي تعمل بها العملية على المستوى الجزيئي. كان على وشك الانتقال من المشروع عندما جعلت تجربة واحدة في وقت متأخر من الليل كل شيء في مكانه.
سم بكتيري يحرر الجينات
يقول دي مورايس إن الأمر كان مثل مسلسل تلفزيوني. لقد اشتبه في وقت مبكر في أن البروتين السام مرتبط بالحمض النووي وقام بتعديل حرف DNA واحد. كان هذا الحرف هو السيتوزين (C)، لذلك كان يشبه حرفًا مختلفًا، الثايمين (T). كانت الأخطاء المطبعية المتعمدة في الحمض النووي هي التي أسقطت ضحايا السموم. لكن ما تعلمه دي مورايس من تلك التجربة المصيرية في وقت متأخر من الليل كان مختلفاً.تعلم أنه على عكس جميع البروتينات الأخرى المحولة للسيتوزين، فإن السم قام بإجراء تغييراتمختلفة. غير الحمض النووي المزدوج الشريطة بدلاً من الحمض النووي أحادي السلسلة. يبدو هذا فرقًا بسيطًا، لكن له آثارًا كبيرة.
حتى الآن، استخدم محررو القواعد بروتينات مثل Cas9 لفصل الحمض النووي المستهدف إلى خيوط مفردة قبل إجراء تغيير. لكن قطع الRNA اللازمة لوظيفة هذه البروتينات لا يمكنها الوصول إلى الميتوكوندريا. المحرر الأساسي الذي يعتمد على توكسين B. cenocepacia، والذي يعمل على الحمض النووي مزدوج الشريط، لن يحتاج بعد الآن إلى الاعتماد على Cas9. حفز احتمال تطوير أداة صديقة للميتوكوندريا محادثات مع ديفيد ليو، عالم الأحياء الكيميائية والباحث في HHMI في جامعة هارفارد ومعهد ماساتشوستس للتكنولوجيا .
مشاكل واجهت البحث
ومع ذلك ، كان الإنزيم الجديد المحول للسيتوزين قاتلًا لخلايا الثدييات كما كان للفريسة البكتيرية. يقول ليو إن الخطوة الأولى في “ترويض الوحش” كانت تعديل السم بحيث لا يفسد الحمض النووي المزدوج الشريطة دون تمييز. قسم الباحثون البروتين إلى أنصاف غير سامة. غيرت القطعتان السيتوزين إلى الثايمين فقط عندما تم جمعهما معًا في نفس بقعة الحمض النووي.
يقول كارلوس مورايس، عالم أحياء الميتوكوندريا بجامعة ميامي بفلوريدا، والذي لم يشارك في هذا العمل: “إنه رائع جدًا”.
لتوجيه نشاط نصفي الإنزيم، أرفق الباحثون بروتينات TALE، وهي قطع قصيرة من البروتين يمكن اختيارها لاستهداف امتدادات معينة من الحمض النووي. في تجارب زراعة الخلايا، نجح محرر الميتوكوندريا في تحويل السيتوزين إلى الثايمين في مواقع الحمض النووي للميتوكوندريا المقصودة. كان العمل ناجحاً بكفاءات تتراوح من 5 إلى 49 في المائة.
سيهدف العمل المستقبلي إلى تحسين الكفاءة، وتطوير أنواع جديدة من محررات الميتوكوندريا التي يمكن أن تنتج تغييرات أخرى في قاعدة الحمض النووي. و بالتالي معرفة ما إذا كان تحرير جينات الميتوكوندريا يعمل في الحيوانات.
يقول شوخرت ميتاليبوف، عالِم بيولوجيا الميتوكوندريا في جامعة أوريغون للصحة والعلوم في بورتلاند، والذي لم يشارك في العمل: “هذه مجرد خطوة أولى”، “لكن في الاتجاه الصحيح.”