مجموعة المعلومات الحيوية الجديدة أعلنت عن توفير برمجيات حديثة للمساعدة في مكافحة كوفيد 19
تطوير اللقاحات و العلاجات و وسائل التشخيص هي اسلحة لمحاربة اي مرض و حاليا الكوفيد 19. كما تم الاعلان سابقاً، أصبحت وكالة العلوم الوطنية الأسترالية جزء أساسيا في رد الفعل العالمي لمكافحة المرض عن طريق تطوير واحد من أول الدراسات الاكلينكية الأولية لفحص اللقاح على المتطوعين. و هو برنامج معلومات حيوية جديد لاختبارات اللقاحات لكوفيد 19.
بروفسور فاسان كان رائد عملية البحث الممولة من ائتلاف الإبتكار للاستعداد لمواجهة الجوائح و جزء من المركز الاسترالي. للاستعداد لمواجهة الامراض والذي سيلعب دوراً هاما في إعداد الأمن البيولوجي في أستراليا و المضي قدماً.
علم الجينات – يغير قواعد اللعبة بالنسبه للدراسات السريرية
استعدادا للمرحلة الما قبل سريرية للقاح، كان العمل على فهم و فك الجين الخاص بهذا الفيروس المستجد. فهو بمثابة البصمة التي تحمل إعدادات الهجوم و التصرف و أنواع الأمراض القادر على التسبب فيها. بينما يعتبر فيروس كوفيد 19 قادراً على التدقيق في ميكانيكية عمله. و لديه القدرة على التحول و التغير ببطء مقارنة بفيروسات اخرى مثل الانفلونزا فان نتائج هذه التغيرات يبقى غير معلموماً. أهمية تحديد الجين كان قد تم مناقشته في عدة أوراق بحثية للحث على إختيار سلالة الفيروس بدقة لتجنب القيام بدراسات سريرية على الفيروس الغير موجود في المجتمع حالياً.
أول فيروس كوفيد 19 تم تحليله
للشرح اكثر قام فريق من مؤسسة “الأمراض العابرة للحدود والناشئة”. بتطوير رسم بياني يشرح كيفية مقدرة الفيروس على التحول عند انتقاله من الحيوان إلى الإنسان عن طريق وسيط حيواني غالبا. ببينما تحليل الجينات يعطينا فكرة عن نوعية الفيروس إلا أن العينات المستخرجه من الانسان تعطينا نبذة عن ماهية الفيروس على أرض الواقع. على سبيل المثال أول فيروس كوفيد 19 تم تحليله (بتحولات برتقالية و وردية). قد يكون شديد الاختلاف عن السلالة الاصلية (الرمادية ) اللون التي كانت تصيب الانسان. مقارنة أيضا بالنوع (الأخضر) والذي تم عزله لاحقا. بالتالي محاولة إختيار سلالة عامة قريبة للنوع المعزول الاولي لاجراء الاختبارات على الحيوانات قد يكون خطأ.
قد يكون هناك أكثر من نوع أو سلالة من الفيروس في المجتمع ممثلة بالألوان المختلفة. و الذين بدورهم قد يكونوا أقل شراسة من النوع (البرتقالي الأزرق و الوردي) والتي يعتبر الأشد فتكا. بالتالي، قد يجب تركيز التشخيص و اللقاح على ايجاد سلالة التي تعتبر الأكثر قربا سريريا أو وبائيا من الأكثر شمولاً. يجب الاخذ بالإعتبار أن الصلة الوبائية قد يصعب حصرها خلال وجود جائحة.
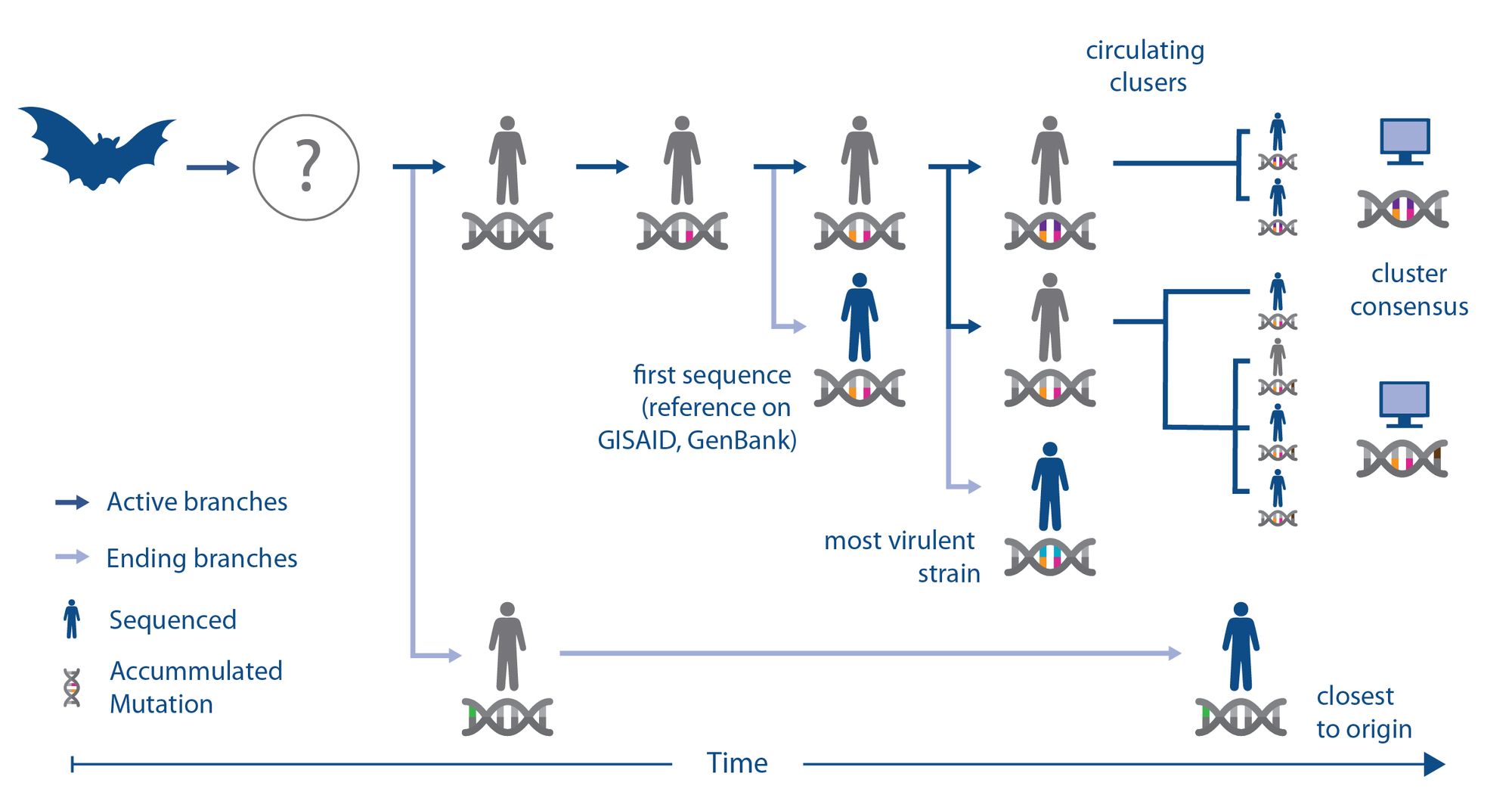
كما هو موضح في الورقة البحثية و من خلال التحليل أصبح واضحاً أن مرجع سارس 2 غالباً ما يكون ممثلا لأول السلالات التي أصابت الإنسان. ولكن أصبح واضحاً أن هنالك العديد من السلالات الموجودة والتي تتمتع بتحولات ثابتة و التي تبقى مجهولة التبعات.
اختيار سلالة فيروس ممثلة
في ظل غياب الشروحات السريرية مثل شدة المرض أو قابلية إنتقاله اختيار السلالة الأنسب للبحوث السريرية ما زال عنواناً مهما للبحث النشيط، خاصة وأن الفيوس مستمر في التطور، إختيار المرجع قد يسبب ظهور نموذج عام ولكن متأخر و قديم. بينما إختيار سلالة حديثة التحول قد يسبب تطوير لقاح يغطي فئة صغيرة من تلك الموجودة والمنتشرة بما لا يكون له أي خواص سريرية مهمة.
باوير و زملاؤه يصرون على أن اختبار السلاسلة يجب أن يكون مبنيا على وجود فروقات جينية صغيرة جداً عن جميع السلالات الموجودة. والتي يجب ان تستمر في العمل حتى نهاية مرحلة الدراسات السريرية والتي قد تمتد لعام أو عام ونص. ولكن هذا صعب جدا في وجود فيروس يحتوي 30000 حرف و اكثر من 10000 عينة معزولة.
المقاربة المعهودة لإنتاج شجرة وراثية للتمكن من رؤية المسافة التطويرية. هنا تحليلات من أفرع مختلفة يفترض أنها أكثر تنوعا من تحليلان على نفس الشجرة. بمعنى أن نوعا معزولاً لديه نفس عدد التحولات من سلالتين مختلفتين فإن الخوارزمية ستضعه بقرب إحدها فقط. هنا تصبح احداث المزج مشكلة، عندما يكون سلالتان متباعدتان قادرتان على إنتاج وليد بصفات ممزوجة. بالإضافة إلى أن إنتاج شجرة وراثية يتطلب الالاف من السلالات القابلة للمعالجه الحاسوبية و الذي يعتبر مكلف جدا و مستحيل أحيانا.
قياسات جينية خالية من قياسات المحاذاة
تم تطوير مقاربة خالية من قياسات المحاذاة قادرة على التاقلم بسرعة مع المخزن التحليلي للفيروس و مقياس لملاين الفيروسات المعزولة.
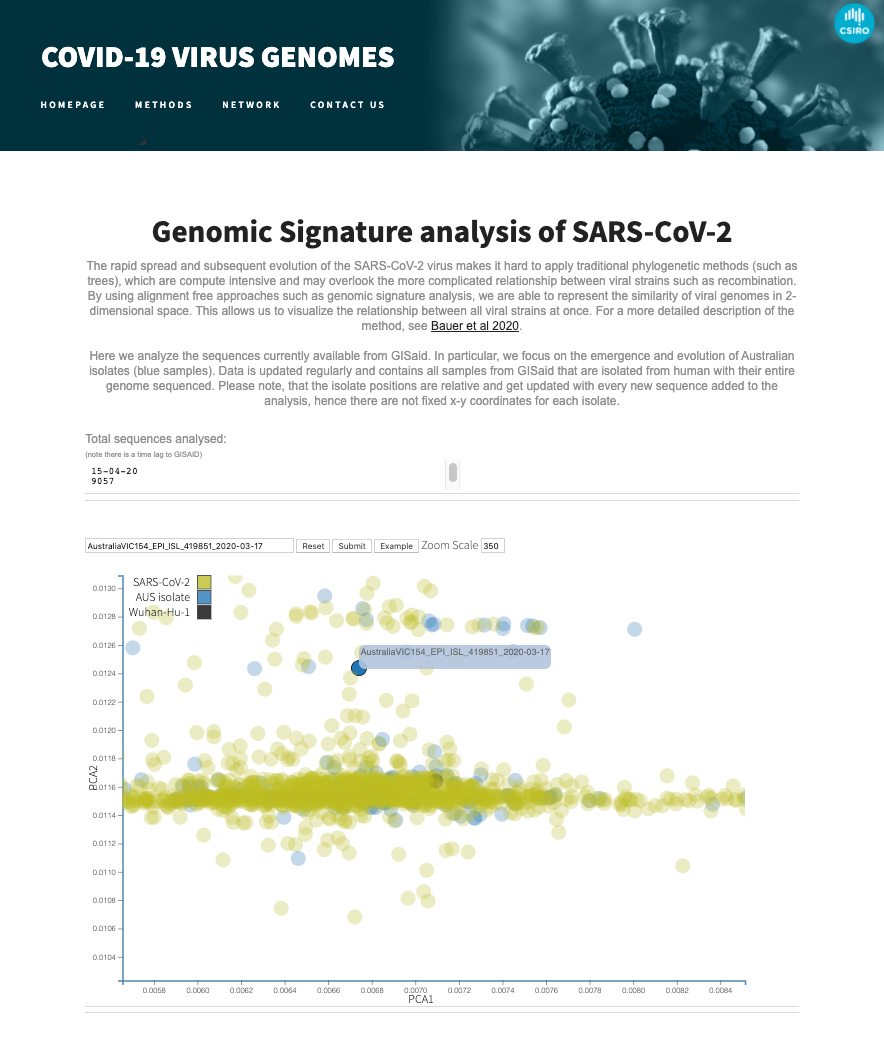
هنا لكل عضو تم عزله يوجد جين مميز مبني على التكوين التحليلي للجينات. لشرح كمية هذا الجين المميز اخترنا تكرار كي-مير “K-mer frequency”. لعد جميع الخيوط الممكنة لطول كي في تكرار الفيرس برز كبديل لشجرة الوراثة. المسافة المفمومة بين جميع المعزولات يمكن تصورها عن طريق إجراء تحليل المكون الرئيسي على الجين المميز للتقليل من تعداد أبعاد وسيط الكي مير الى كون ثنائي الأبعاد. في الورقة الثانية طبقنا هذه الوسيلة لجميع التكرارات لسارس 2 لرسم خريطة المسافه المتطورة المزعومة للفيروس و اختيار سلالة ممثلة للاستجابة الاسترالية للكوفيد 19.
تصور عدد التكرارات المتزايد للكوفيد سارس 2
لتمكين الباحثين الأخرين لتصوير التكرار المتنامي لل جيسيد، قمنا بإطلاق خدمة شبكية توفر رؤية حقيقية وقتية للمنظر للجيني لفيروس سارس 2.